И вот, готовясь к лекциям на очередном интенсиве по анализу выживаемости набрела на раздел FAQ по пакету adjustedCurves, который используется для оценки скорректированной выживаемости1. Ниже один из вопросов оттуда и ответ Робина Денца, главного разработчика пакета, на него.
Q: Can I use this package if the variable I am interested in is continuous?
A: It is possible, but not recommended. To get adjusted survival curves or CIFs for a continuous variable of interest with this package, users need to categorize the variable before doing any kind of analysis. This leads to a loss of information, which may lead to biased estimates or a loss of statistical power. To circumvent this issue, we developed another R-package called contsurvplot which directly implements plotting methods for continuous variables, as described in Denz & Timmesfeld (2023).
Оказалось, что аналог adjustedCurves для визуализации оценок выживаемости (как Каплана-Мейера, так и скорректированных) в зависимости от количественных показателей существует вот уже несколько лет и имя ему contsurvplot, и главный разработчик его – тот же Робин Денц.
У обоих пакетов довольно содержательные странички на GitHub: вот для adjustedCurves, а вот для contsurvplot. По сути, все возможные способы визуализации для количественных показателей описаны и сопровождены примерами в разделе Articles на той же страничке и в статье Denz et. al (2023). В последней, помимо этого, перечислены все методы коррекции, с результатами которых позволяет работать данный пакет, а также представлены результаты симуляций для сравнения методов и сценариев коррекции по смещению полученной оценки эффекта относительно его истинного значения и показателям качества.
Технически есть следующие способы визуализации оценки выживаемости в зависимости от значений количественного предиктора/ воздействия (картинки взяты со странички пакета contsurvplot, количественная переменная – число пораженных лимфатических узлов – называется nodes):
1️⃣ “Двумерные” графики
-
Зависимость оценки выживаемости в одной или несольких временнЫх точках (t) от значения количественной ковариаты:
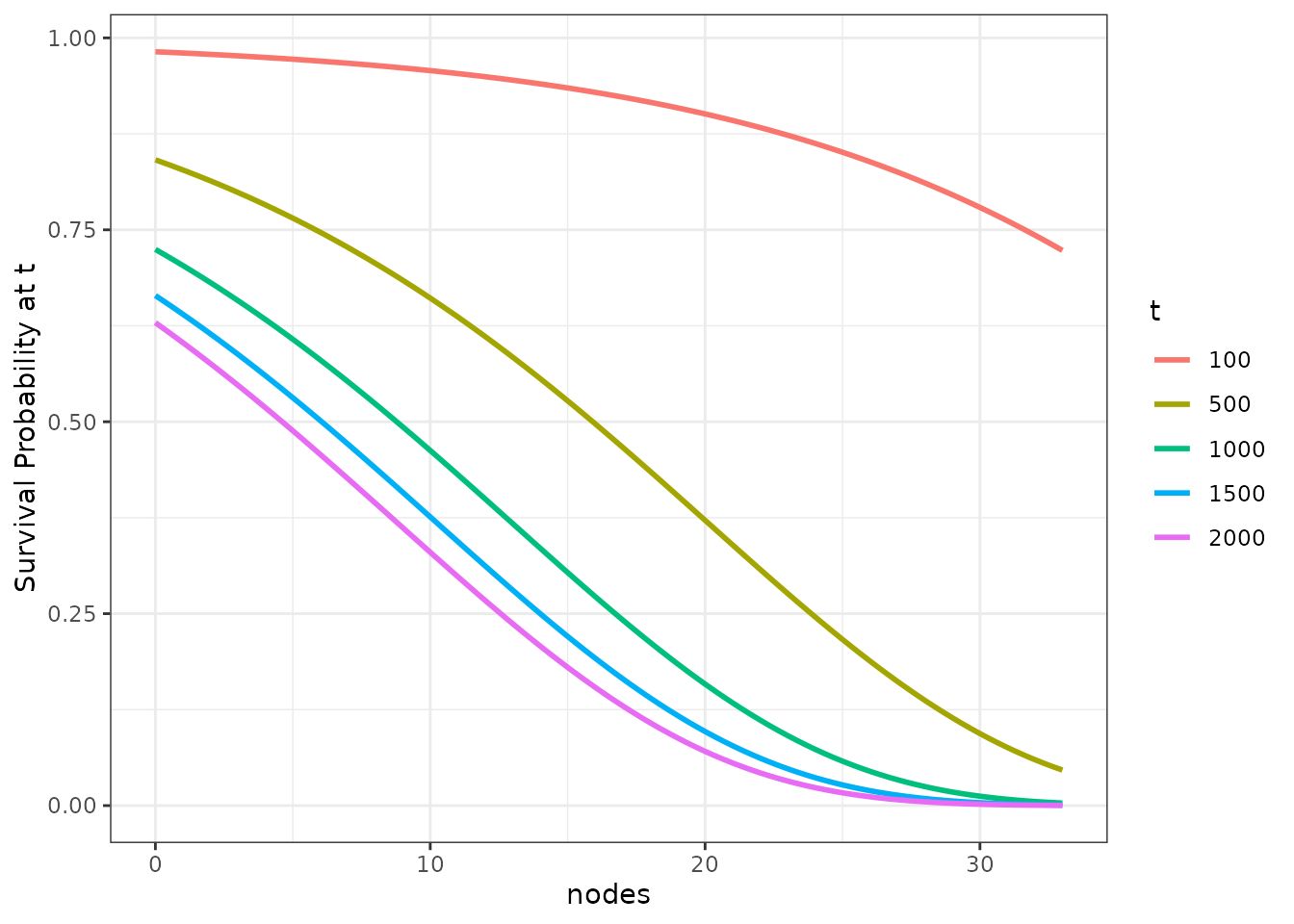
-
Зависимость любого квантиля выживаемости (например, медианы) (p) или средней ожидаемой продолжительности жизни без события за определенный период времени (RMST) от значения количественной ковариаты:
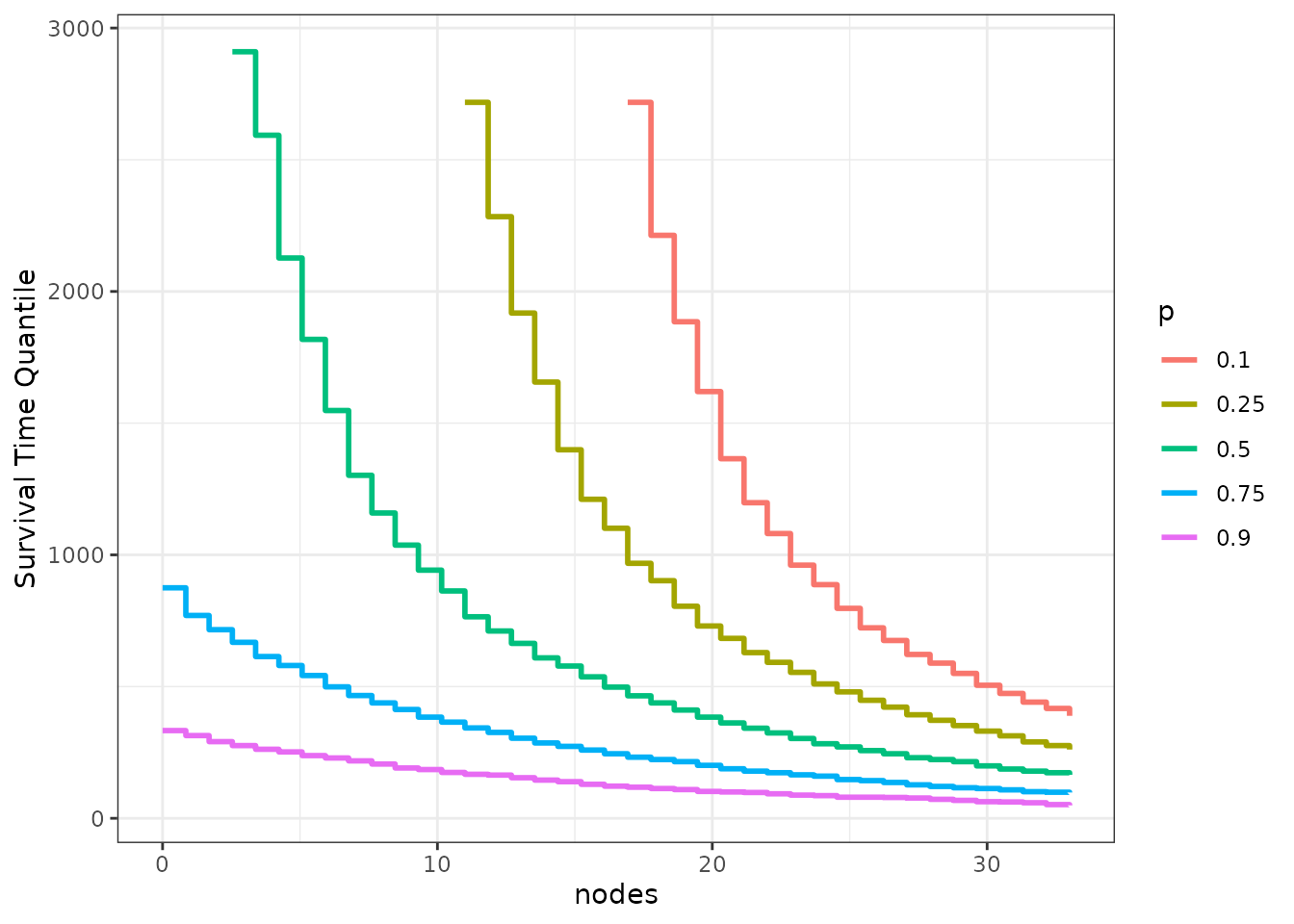
-
Кривые выживаемости для одного или нескольких значений количественного признака:
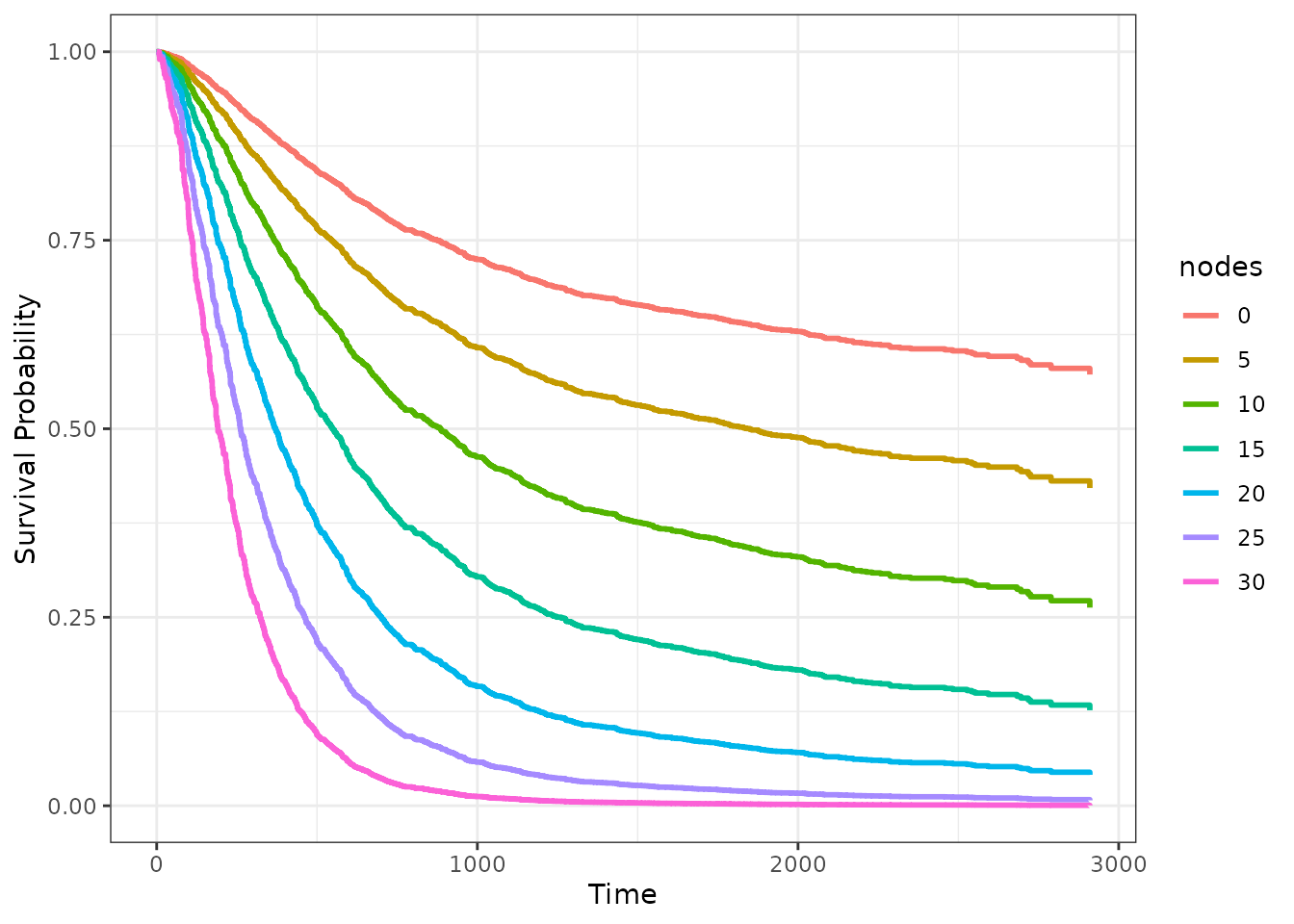
2️⃣ “Трёхмерные” графики – разработчики пакета рекомендуют использовать именно их, как наиболее информативные; можно и 3D поверхности изобразить, однако они обычно сложны для восприятия, поэтому третья ось обычно отображается с помощью цветовой заливки
-
Контурные графики выживаемости: по оси X – время, по оси Y – значение количественного признака, цвет заливки – в зависимости от значения выживаемости (S(t)) при соответствующем сочетании времени оценки и значения ковариаты:
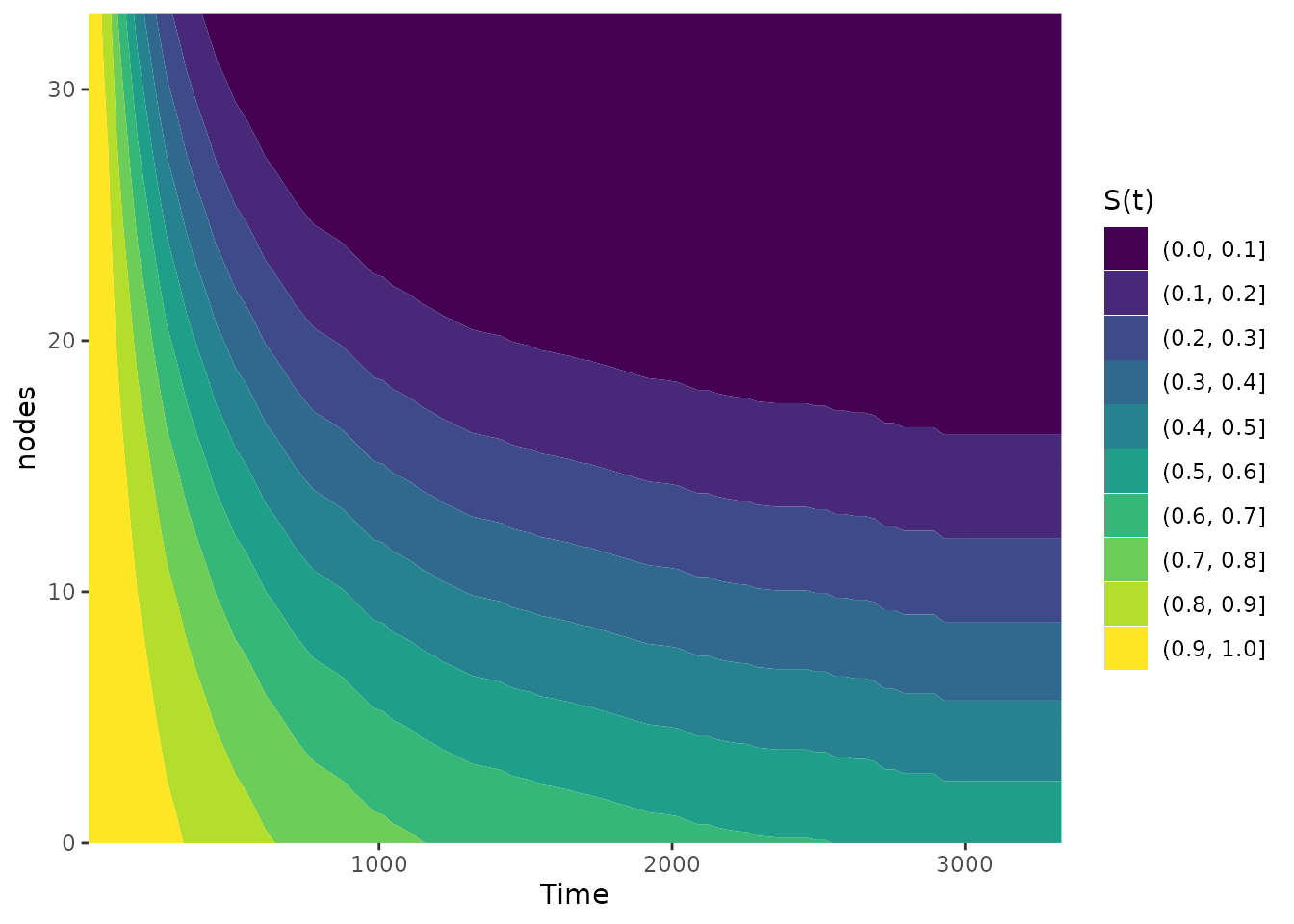
-
“Трёхмерные” кривые Каплана-Майера: по оси X – время, по оси Y – значение выживаемости, цвет заливки – в зависимости от значения количественного признака:
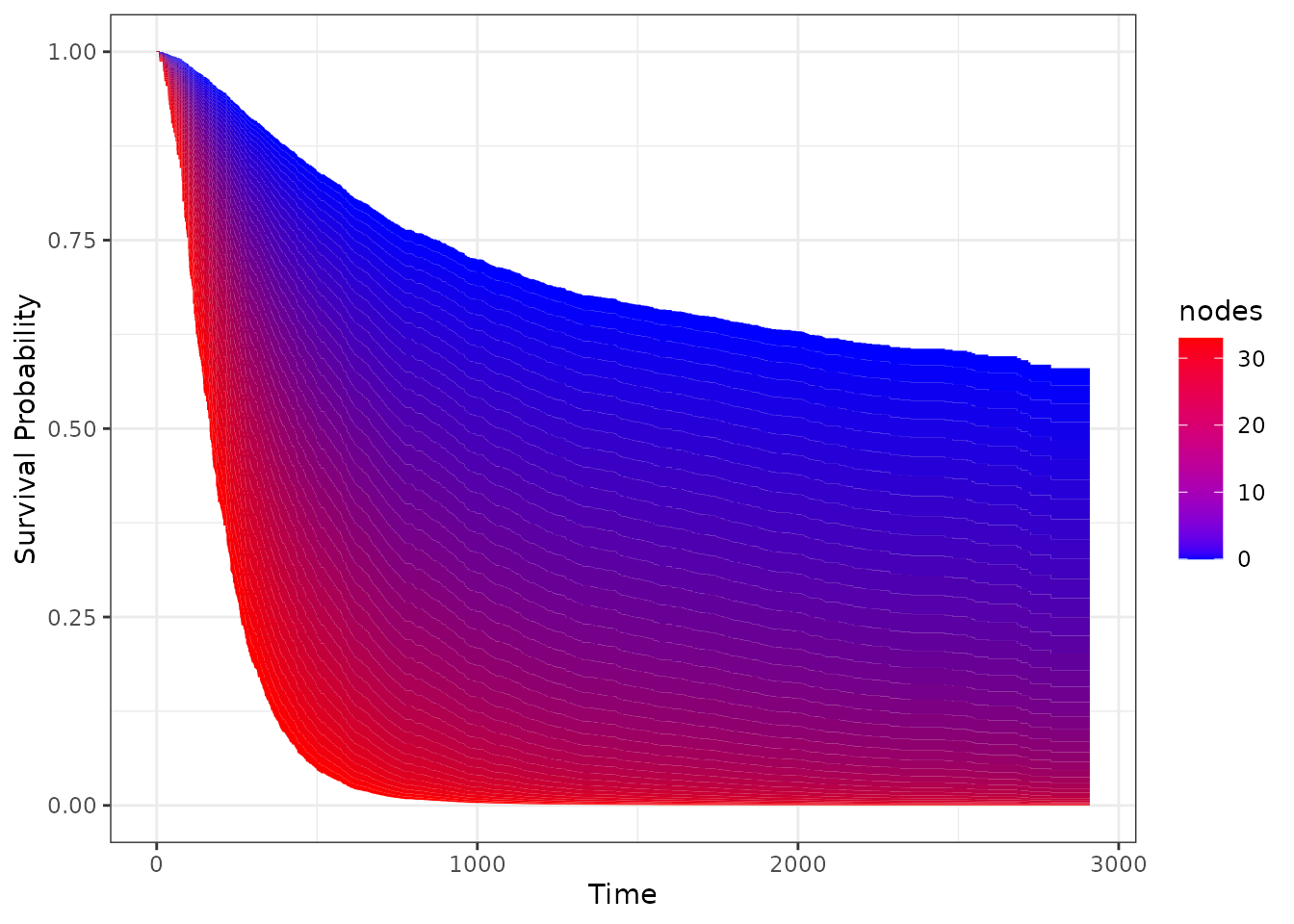
Красота, я считаю! 😍
-
С коррекцией на ковариаты, выполненной разными методами, включая регрессию, мэтчинг, взвешивание и даже инструментальные переменные ↩